Der pH-Wert dient als Maß für den sauren bzw. basischen Charakter einer wässrigen Lösung.
Der Begriff leitet sich vom lateinischen „potentia hydrogenii“ (=die Kraft/Stärke des Wasserstoffs) ab und gibt die Wasserstoffionenkonzentration in g/Liter an. Werden Säuren oder Basen in Wasser gelöst, geben diese durch Dissoziation Wasserstoffionen ab und verändern dadurch den pH-Wert. Damit wird der pH-Wert zu einem Parameter für die Menge an Säuren oder Basen in einer Lösung.
Die Wasserstoffionenkonzentration einer Flüssigkeit gibt an, ob sie sauer, basisch oder neutral ist.
Der Neutralpunkt liegt bei 10 hoch -7 mol/Liter. Ist der Wert höher, reagiert die Flüssigkeit sauer, ist er niedriger, verhält sich dagegen basisch.
Zur Vereinfachung versieht man den Exponenten mit einem positiven Vorzeichen und bezeichnet diesen als pH-Wert zwischen 0 und 14:
- pH-Wert < 7 sauer
- pH-Wert = 7 neutral
- pH-Wert > 7 basisch
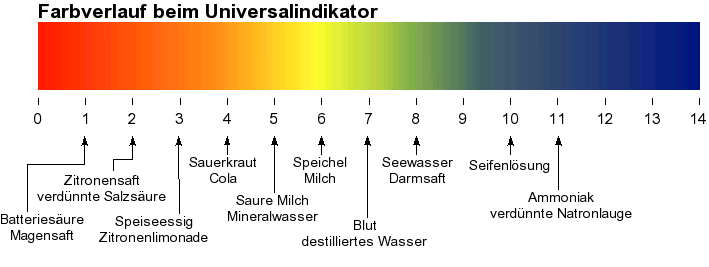
Genau bestimmt werden kann der pH-Wert mit Hilfe von bestimmten Messgeräten (pH-Elektrode) oder ungefähr mit einem Universal-Indikator und dem Vergleich mit einer Farbskala.
Von Bedeutung im Zusammenhang mit Wasser ist der pH-Wert, da die Toleranz der meisten Organismen gegenüber pH-Schwankungen in ihrem Lebensraum relativ gering ist.
Optimal ist für die meisten Lebewesen der Bereich zwischen 7,5 und 8,5.
Gemäß der Trinkwasserverordnung muss Trinkwasser einen pH-Wert zwischen 6,5 und 9,5 aufweisen.